Tóm tắt tài liệu
Trong chương 1 của hóa học lớp 10 về nguyên tử, thành phần nguyên tử là bài mở đầu. Do đó, bài này mang đến cho các em học sinh khá nhiều kiến thức cơ bản nhưng không kém phần quan trọng. Vậy nguyên tử có những thành phần nào cấu thành? Lịch sử khám phá ra sao? Chương này có những dạng bài tập nào, hãy khám phá ngay dưới bài viết sau đây
Tóm tắt kiến thức cơ bản
Sự khám phá ra electron
Năm 1897, nhà vật lí Anh Tôm-xơn khi nghiên cứu hiện tượng phóng điện trong khí loãng đã phát hiện ra tia âm cực, mà bán chất là chùm các hạt nhó bé mang diện lích âm, gọi là electron, ký hiệu là e.
Sự khám phá ra hạt nhân nguyên tử
Năm 1911, Rơ-dơ-pho dã làm thí nghiệm cho một chùm hạt a mang diện tích dương bắn vào một lá vàng mỏng (khoảng 10 mm) dặt trước màn huỳnh quang, chứng minh sự tồn tại cùa hạt nhân nguyên tử.
Kết quả thí nghiệm cho chúng ta đưa ra các nhận xét sau đây:
- Nguyên tử có cấu tạo rỗng.
- Hạt nhân có kích thước rất nhỏ so với kích thước nguyên tử.
Sự khám phá ra proton
Năm 1919, Rơ-dơ-pho phát hiên ra trong hạt nhân nguyên từ có loại hạt mang diện tích dương, được gọi là proton. Đó chính là ion dương H+, kí hiệu là p (proton).
Sự khám phá ra natron
Bâng thực nghiêm, dùng chùm a bắn phá tấm kim loại beri (Bc) mỏng, Chat-vich (cộng tác vièn của Ro-dơ-pho) dã phát hiện ra loại hạt vi inô có khà nàng xuyên thủng rất lớn, có khối lượng xấp xỉ proton d nhưng không mang diện tích. Đó là hạt nơtron, kí hiệu là n.
Kết luận
Thành phần cấu tạo nguyên tử gồm:
- Hạt nhân tích điên dương, nằm ở tâm nguyôn từ. Hạt nhân đượccâu tạo hởi các proton (p) và các nơtron (n).
- Vỏ electron cùa nguyên tử gồm các electron tích điện âm, chuyếnđộng xung quanh hạt nhân.
- Điện tích của electron và của proton đều rất nhỏ:
+ Điên tích của electron : qe= -1,602.10^-19 culông.
+ Điên tích của proton : qp = +1,602.10^-19 culông.
Như vậy, điên tích của electron và của proton có trị số là bằng nhau nhưng ngược dấu nhau.
+ 1,602.10^-19 culông là giá trị điện tích nhỏ nhất nên được gọi là điện tích nguyên tử và được dùng làm đơn vị điện tích.
Nghĩa là : qe = -1 và qp = +1.
- Nơtron là hạt không mang điên (qn = 0).
Khối lượng nguyên tử
Bằng thực nghiêm người ta đã xác định được khối lượng các hạt có trong thành phẩn nguyên tử:
+ Khối lượng electron : me = 9,1095.10^-31 kg.
+ Khối lượng proton : mp = 1,6726.10^-27 kg.
+ Khối lượng nơtron : mn = 1,6748. 10^-27 kg.
Proton và nơtron có khối lượng xấp xỉ bằng nhau, còn electron có khối lượng rất bé, chỉ gần bằng 1/1804 khối lượng của proton (hoặc nơtron). Do vây, khối lượng của nguyên từ chủ yếu tập trung ờ hạt nhân. Hay nói một cách khác : khối lượng cùa hạt nhân được coi là khối lượng nguyên từ.
- Vì khối lượng nguyên từ vồ cùng nhò bé, để tiôn sử dụng, người ta đưara đơn vị kliôì lượng nguyên tử quy ước là đơn vị cacbon (viết tát là dvC).
- Khối lượng nguyên từ tính bằng đơn vị cacbon gọi là nguyên từ khối.
- Nguyên tử khối là khối lượng tương dối cùa nguyên từ.
Kích thước nguyên tử
Nếu hình dung nguyên tử như một quả cẩu, trong đó có các electron chuyển dộng rất nhanh xung quanh hạt nhân, thì dường kính của quả cầu đó khoảng 10^-10 m.
Để biểu thị kích thước nguyên từ, người la dùng dơn vị Angxtrom, kí hiệu là A và nanomel, kí hiệu là nm:
1A = 10^-10m và lnm= 10^-9m = 10Â.
Nguyên tử nhỏ nhất là nguyên tử hidro, có hán kính khoáng 0.53Ă.
Đường kính cứa hạt nhân nguyên tứ còn nhó hơn nhiều, vào khoáng 10^-4Ầ.
Như vậy dường kính nguyên tử lớn hơn dường kính cùa hạt nhân khoáng 10.000 lân. Nêu ta hình dung hạt nhân nguyên tử là quá CẦU có bán kính 5cm (như quả cam) thì nguyên từ là một quá cầu có dường kính tới 1000m = 1Km.
Hướng dẫn giải bài tập trong sgk
1. Câu đúng là B.
2. Câu đúng là D.
3.
mNe = 20.180 . 1,66 . 10^-27 = 33,4988 . 10^-27
Khi điện phân nước, thu được sô nguyên từ H gấp đôi số nguyên tử O.
Như vậy 1 nguyên oxi có khối lượng gấp 2.7,937 = 15,874 lẩn khối lượng nguyên tử H.
mO = 15.874.( 1,0080.1,66.10^-27) = 26.562.10^-27kg
Đáp số: 15,99 dvC.
Bài tập có hướng dẫn giải
1.1 Trong 7 gam nitơ có bao nhiêu gam electron, proton? Biết một mol nguyên tử nitơ có khối lượng 14 gam, một nguyên tử nitơ có 7 electron
1.2 Tính khối lượng 1 mol electron, một mol proton, Biết khối lượng của electron me = 9,1.10^-28 gam, khối lượng của proton mp = 1,67.10^-24.
1.3 Trong 0,64 gam lưu huỳnh có bao nhiêu gam proton, bao nhiêu gam electron ? Biết khối lượng mol của lưu-huỳnh là 32 gam, trong nguyên tử lưu huỳnh, số proton bằng số nơtron.
1.4 Biết khối lượng của electron bằng 9,1.1031kg, của proton bằng 1,67.1027. Hãy tính khối lượng của proton và electron theo đơn vị cacbon.
1.5 Tính bán kinh gần đúng cùa nguyên tử canxi, biết rằng 1 mol canxi chiếm thể tích là 25,87 cm3 và trong tinh thể, các nguyên tử canxi chỉ chiếm 74
Bài tập tự luận có đáp án
1.6 Cho biết khối lượng nguyên tử của ba nguyên tố: Heli (He), Neon (Ne) và urani (U) là:
mHe = 6.65.10^-24 gam ;
mNe = 33,2.10^-24 gam;
mu = 395,30.10^-24 gam;
a) Tính tỷ số khối lượng của các electron so với khối lượng của toàn bộ nguyên tử trong mỗi trường hợp.
b) Có thể coi khối lượng nguyên tử bằng khối lượng cùa hạt nhân được không ?
Đáp số
a) 2.74.10^-4; 2.74.10^-4; 2.1.10^-4
b) Có thể
1.7 Nguyên tử sắt có ký hiệu như sau : 56/26Fe
a) So sánh khối lượng của các electron có mặt trong nguyên tử với khối lượng của toàn nguyên tử.
b) Tính khối lượng của các electron trong 1 kg sắt.
c) Tính khối lượng của sắt chứa 1 kg electron.
Đáp số
a) 2,5.10^-4;
b) 0,255 g ;
c) 3920 kg sắt.
1.8
a) Khi nguyên tử natri (Na) mất đi một electron, nó biến thành ion natri với ký hiệu là Na+.
b) Khi nguyên tử oxi (‘ jO) nhận thêm hai electron, nó biến thành ion o2. Tính tỷ số khối lượng của electron mất đi hay thu vào so với khối lượng của toàn nguyên tử. Nhận xét.
Đáp số
a) 2,4.10^-5;
b) 6,8.10^-5: Khi nguyên tử mất đi hoặc thu vào một số electron thì khối lượng nguyên tử coi như không thay đổi.
1.9 Electron của nguyên tử hiđro chuyển động bên trong hình cẩu có bán kính 3.10^-8cm (Chỉ có một phần nghìn khả năng tìm thấy nó ở ngoài hình cầu).
Hạt nhân nguyên tử hiđro coi như một quả cầu có bản kính lả 5.10^-13 cm.
Nếu phóng đại hạt nhân lên bằng quả cam có đường kinh 6 cm thì bản kính nguyên tử sẽ là bao nhiêu ?
Đáp số: 1800m
Bài tập trắc nghiệm
Câu 1: Nguyên tử X có 26 proton trong hạt nhân. Cho các phát biểu sau về X:
X có 26 nơtron trong hạt nhân.
X có 26 electron ở vỏ nguyên tử.
X có điện tích hạt nhân là 26+.
Khối lượng nguyên tử X là 26u. Trong các phát biểu trên, có bao nhiêu phát biểu đúng?
A. 1. B. 2. C. 3. D. 4.
Câu 2: Nguyên tử vàng có 79 electron ở vỏ nguyên tử. Điện tích hạt nhân của nguyên tử vàng là (kí hiệu của vàng là Au)
A. +79. B. -79. C. -1,26.10-17 C. D. +1,26.10-17 C.
Câu 3: Một nguyên tử có 12 proton và 12 nơtron trong hạt nhân. Điện tích của ion tạo thành khi nguyên tử này bị mất 2 electron là gì? Chọn câu trả lời đúng trong các câu sau
A. 2+. B. 12+. C. 24+. D. 10+.
Câu 4: Nguyên tử natri có 11 electron ở vỏ nguyên tử và 12 nơtron trong hạt nhân. Cho biết rằng tỉ số khối lượng giữa hạt nhân và nguyên tử natri là
A. ≈ 1,0. B. ≈ 2,1. C. ≈ 0,92. D. ≈ 1,1.
Câu 5: Tưởng tượng ta có thể phóng đại hạt nhân thành một quả bóng bàn có đường kính 4 cm thì đường kính của nguyên tử là bao nhiêu? Cho biết rằng đường kính của nguyên tử lớn hơn đường kính của hạt nhân khoảng 104 lần. Tức là vào khoảng 10.000 lần. Chọn phương án đúng trong các phương án sau:
A. 4m. B. 40 m. C. 400 m. D. 4000 m.
Câu 6: Một nguyên tử chỉ có 1 electron ở vỏ nguyên tử và hạt nhân nguyên tử có khối lượng là 5,01.10-24 gam. Số hạt proton và hạt nơntron trong hạt nhân nguyên tử này lần lượt là bao nhiêu?
A. 1 và 0.
B. 1 và 2.
C. 1 và 3.
D. 3 và 0.
Câu 7: Cho biết nguyên tử crom có khối lượng 52u, bán kính nguyên tử này bằng 1,28 Å. Hãy trả lời các câu hỏi dưới đây:
a) Khối lượng riêng của nguyên tử crom là
A. 2,47 g/cm3.
B. 9,89 g/cm3.
C. 5,20 g/cm3.
D. 5,92 g/cm3.
b) Coi khối lượng của nguyên tử tập trung trong hạt nhân. Khối lượng riêng của hạt nhân nguyên tử crom là
A. 2,31.1011 kg/cm3.
B. 1,38.1014 kg/cm3.
C. 2,89.1010 kg/cm3.
D. 2,31.1013 kg/cm3.
Câu 8: Bắn một chùm tia α đâm xuyên qua một mảnh kim loại. Khi 1 hạt nhân bị bắn phá, có khoảng bao nhiêu hạt α đã đi xuyên qua nguyên tử? Cho biết rằng đường kính nguyên tử lớn hơn đường kính của hạt nhân khoảng 104 lần, tức là khoảng 10.000 lần. Chọn đáp án đúng:
A. 106.
B. 107.
C. 108.
D. 109.
Đáp án chi tiết
| 1. B | 2. D | 3. A | 4. A | 5. C | 6. B | 7. a) B. b) D | 8. C |
Lời giải
Câu 1
Phát biểu 2 và 3 đúng.
Câu 2
Điện tích hạt nhân là +1,26.10-17 C, hoặc kí hiệu là 79+.
Câu 4
Nguyên tử Na có 11 electron ở lớp vỏ nguyên tử, 11 proton và 12 nowtron trong hạt nhân.
Vì me ≈ 9,1. 10-31 kg và mn ≈ mp ≈ 1,67.10-27 kg.
me ≪ mn và mp.
Như vậy, coi như khối lượng nguyên tử tập trung ở hạt nhân.
Câu 5
Nếu đường kính hạt nhân là 4cm thì đường kính nguyên tử khoảng:
4.104 cm = 400 m
Câu 6
Tổng số hạt n và p trong hạt nhân nguyên tử này là:
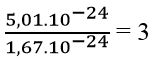
Nguyên tử có 1 electron ở lớp vỏ nguyên tử nên sẽ có 1 proton trong hạt nhân. Suy ra số hạt nowtron trong hạt nhân là 2.
Câu 7:
Coi nguyên tử crom là hình cầu, thể tích nguyên tử là
V=(4/3) πr3 = 8,78. 10-24 (cm3)
Vậy khối lượng riêng của nguyên tử là
D = m/V = (52.1,67.10-24)/(8,78. 10-24 ) = 9,89 (g/cm3)
Thực tế coi nguyên tử là một quả cầu rỗng, khối lượng tập trung ở hạt nhân.
Thể tích hạt nhân là : V = 4/3 πr3= 3,76.10-39 (cm3)
Vậy khối lượng riêng của hạt nhân là :
D = m/V = (52.1,67.10-27)/(3,76.10-39 ) = 2,31.10-13 (kg/cm3)
Với lượng kiến thức cực kì nhiều trong sách giáo khoa. Tuy nhiên, khi tiếp cận chương nguyên tử ở bài số 1 về thành phần nguyên tử, chúng ta chỉ cần nắm vững một số bài tập trắc nghiệm trong bài thôi nhé. Còn lại thì xem cho biết chứ khá là ít khi ra thi. Việc nắm vững chương này sẽ giúp chúng ta giải quyết bài toán nhanh gọn hơn, học các dạng mới cũng dễ dàng hơn.
Tham khảo
1. https://www.youtube.com/watch?v=q91j9ayJ0FE
2. https://vi.wikipedia.org/wiki/Nguy%C3%AAn_t%E1%BB%AD
Xem thêm video
(Lý thuyết thành phần nguyên tử)



 056.3753648
056.3753648
 Chat FB
Chat FB